本指導(dǎo)原則旨在指導(dǎo)注冊(cè)申請(qǐng)人對(duì)人工復(fù)蘇器(俗稱:簡(jiǎn)易呼吸器)注冊(cè)申報(bào)資料的準(zhǔn)備及撰寫(xiě)�����,指導(dǎo)和規(guī)范人工復(fù)蘇器的技術(shù)審評(píng)工作��,幫助審評(píng)人員理解和掌握該類產(chǎn)品結(jié)構(gòu)���、性能�����、預(yù)期用途等內(nèi)容����,把握技術(shù)審評(píng)工作基本要求和尺度����,對(duì)產(chǎn)品安全性、有效性作出系統(tǒng)評(píng)價(jià)����。
本指導(dǎo)原則所確定的核心內(nèi)容是在目前的科學(xué)認(rèn)知水平和產(chǎn)品技術(shù)基礎(chǔ)上形成的。因此����,注冊(cè)申請(qǐng)人和審評(píng)人員應(yīng)注意其適宜性,密切關(guān)注適用標(biāo)準(zhǔn)及相關(guān)技術(shù)的[敏感詞]進(jìn)展�,考慮產(chǎn)品的更新和變化。
本指導(dǎo)原則不作為法規(guī)強(qiáng)制執(zhí)行,不包括行政審批要求�。注冊(cè)申請(qǐng)人和審評(píng)人員需密切關(guān)注相關(guān)法規(guī)的變化,確認(rèn)申報(bào)產(chǎn)品是否符合法規(guī)要求�。
適用范圍
本指導(dǎo)原則適用于人工復(fù)蘇器,該產(chǎn)品用于實(shí)施人工呼吸��、急救時(shí)提供肺通氣�����。根據(jù)《醫(yī)療器械分類目錄》(G家食品藥品監(jiān)督管理總局公告2017第104號(hào))���,人工復(fù)蘇器的管理類別為二類�����,分類編碼為08—03—05(呼吸����、麻醉和急救器械—急救設(shè)備—人工復(fù)蘇器(人工復(fù)蘇器))���。
本指導(dǎo)原則范圍不適用電動(dòng)�����、氣動(dòng)復(fù)蘇器��。
技術(shù)審查要點(diǎn)
產(chǎn)品名稱要求
人工復(fù)蘇器產(chǎn)品命名應(yīng)符合《醫(yī)療器械通用名稱命名規(guī)則》([敏感詞]食品藥品監(jiān)督管理總局令第19號(hào))���、《醫(yī)療器械分類目錄》和行業(yè)標(biāo)準(zhǔn)中的通用名稱,如“人工復(fù)蘇器”��、“簡(jiǎn)易呼吸器”����。
產(chǎn)品的結(jié)構(gòu)和組成
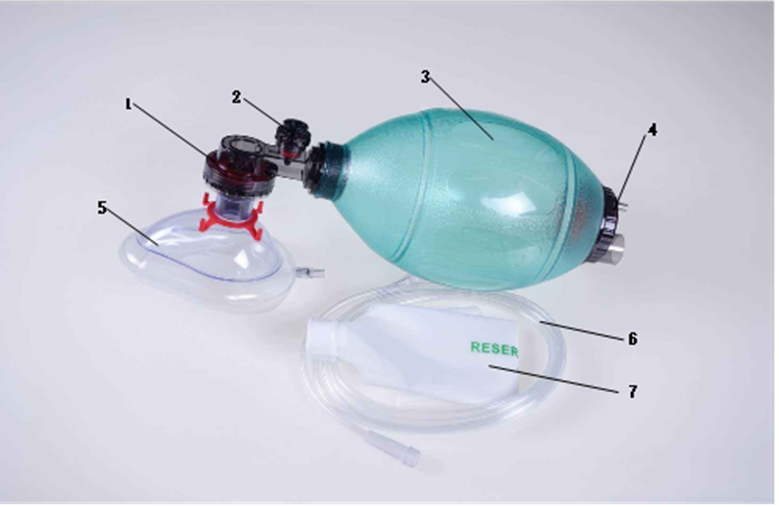
人工復(fù)蘇器通常由病人閥(可含限壓閥)、呼吸球囊��、進(jìn)氣閥組組成����。可根據(jù)不同的使用要求配置各種相應(yīng)的選配件�����,如面罩���、氧氣管��、儲(chǔ)氣袋或儲(chǔ)氣管等�����。按照使用次數(shù)可以分為可重復(fù)使用�、一次性使用產(chǎn)品。產(chǎn)品結(jié)構(gòu)示意圖如下:
1-病人閥 ����; 2-限壓閥; 3-呼吸球囊���; 4-進(jìn)氣閥組���;5-面罩(選配); 6-氧氣管(選配)�����; 7-儲(chǔ)氣袋(選配)
圖1 人工復(fù)蘇器示意圖
產(chǎn)品工作原理/作用機(jī)理
人工復(fù)蘇器產(chǎn)品主要用于實(shí)施人工呼吸����、急救時(shí)提供肺通氣。使用時(shí)�,按壓呼吸球囊��,進(jìn)氣閥組關(guān)閉�����,氣體經(jīng)病人閥端進(jìn)入患者呼吸道�;釋放呼吸球囊���,病人閥關(guān)閉,在壓力差作用下��,外界空氣經(jīng)進(jìn)氣閥組進(jìn)入球囊���。當(dāng)需要高濃度氧氣輸送時(shí)����,復(fù)蘇器連接氧氣管���、儲(chǔ)氣袋或儲(chǔ)氣管使用�,通過(guò)氧氣管接頭連接氧氣源�����,儲(chǔ)氣袋充滿氧氣后,過(guò)量氧氣通過(guò)進(jìn)氣閥組排出到空氣中����。
注冊(cè)單元?jiǎng)澐值脑瓌t和實(shí)例
人工復(fù)蘇器注冊(cè)單元原則上以產(chǎn)品的技術(shù)原理、結(jié)構(gòu)組成�、性能指標(biāo)和適用范圍為劃分依據(jù)。
例:一次性使用人工復(fù)蘇器和重復(fù)使用人工復(fù)蘇器劃分為不同注冊(cè)單元�����;無(wú)菌人工復(fù)蘇器和非無(wú)菌人工復(fù)蘇器劃分為不同注冊(cè)單元���。
產(chǎn)品適用的相關(guān)標(biāo)準(zhǔn)
如表1列出人工復(fù)蘇器主要涉及的現(xiàn)行有效的[敏感詞]/行業(yè)標(biāo)準(zhǔn)���、國(guó)際標(biāo)準(zhǔn);如有標(biāo)準(zhǔn)發(fā)布或更新��,應(yīng)當(dāng)考慮新版標(biāo)準(zhǔn)的適用性����。
表1 產(chǎn)品適用標(biāo)準(zhǔn)(統(tǒng)一格式,標(biāo)準(zhǔn)編號(hào))
|
標(biāo)準(zhǔn)編號(hào)
|
標(biāo)準(zhǔn)名稱
|
|
GB/T 191—2008
|
包裝儲(chǔ)運(yùn)圖示標(biāo)志
|
|
GB 18280.1-2015
|
醫(yī)療保健產(chǎn)品滅菌 輻射 第1部分:醫(yī)療器械滅菌過(guò)程的開(kāi)發(fā)、確認(rèn)和常規(guī)控制要求
|
|
GB 18280.2-2015
|
醫(yī)療保健產(chǎn)品滅菌 輻射 第2部分:建立滅菌劑量
|
|
GB/T 18280.3-2015
|
醫(yī)療保健產(chǎn)品滅菌 輻射 第3部分:劑量測(cè)量指南
|
|
GB 18279.1-2015
|
醫(yī)療保健產(chǎn)品滅菌 環(huán)氧乙烷 第1部分:醫(yī)療器械滅菌過(guò)程的開(kāi)發(fā)、確認(rèn)和常規(guī)控制的要求
|
|
GB/T 18279.2-2015
|
醫(yī)療保健產(chǎn)品的滅菌 環(huán)氧乙烷 第2部分:GB 18279.1應(yīng)用指南
|
|
GB/T 19633.1-2015
|
最終滅菌醫(yī)療器械包裝 第1部分:材料����、無(wú)菌屏障系統(tǒng)和包裝系統(tǒng)的要求
|
|
GB/T 19633.2-2015
|
最終滅菌醫(yī)療器械包裝 第2部分:成形���、密封和裝配過(guò)程的確認(rèn)的要求
|
|
GB/T 14233.1-2008
|
醫(yī)用輸液�、輸血、注射器具檢驗(yàn)方法第1部分:化學(xué)分析方法
|
|
GB/T 14233.2-2005
|
醫(yī)用輸液�、輸血、注射器具檢驗(yàn)方法第2部分:生物學(xué)試驗(yàn)方法
|
|
GB/T 16886.1-2011
|
醫(yī)療器械生物學(xué)評(píng)價(jià) 第1部分:風(fēng)險(xiǎn)管理過(guò)程中的評(píng)價(jià)與試驗(yàn)
|
|
GB/T 16886.5-2017
|
醫(yī)療器械生物學(xué)評(píng)價(jià) 第5部分:體外細(xì)胞毒性試驗(yàn)
|
|
GB/T 16886.7-2015
|
醫(yī)療器械生物學(xué)評(píng)價(jià) 第7部分:環(huán)氧乙烷滅菌殘留量
|
|
GB/T 16886.10-2017
|
醫(yī)療器械生物學(xué)評(píng)價(jià) 第10部分:刺激與遲發(fā)型超敏反應(yīng)試驗(yàn)
|
|
GB/T 16886.12-2017
|
醫(yī)療器械生物學(xué)評(píng)價(jià) 第12部分:樣品制備與參照樣品
|
|
YY/T 0287-2017
|
醫(yī)療器械質(zhì)量管理體系用于法規(guī)的要求
|
|
YY/T 0313-2014
|
醫(yī)用高分子產(chǎn)品包裝和制造商提供信息的要求
|
|
YY/T 0316-2016
|
醫(yī)療器械風(fēng)險(xiǎn)管理對(duì)醫(yī)療器械的應(yīng)用
|
|
YY/T 0466.1-2016
|
醫(yī)療器械用于醫(yī)療器械標(biāo)簽����、標(biāo)記和提供信息的符號(hào)第1部分:通用要求
|
|
YY/T 1474-2016
|
醫(yī)療器械可用性工程對(duì)醫(yī)療器械的應(yīng)用
|
|
YY 0600.4-2013
|
醫(yī)用呼吸機(jī) 基本安全和主要性能專用要求 第4部分:人工復(fù)蘇器
|
|
YY/T 1040.1-2015
|
麻醉和呼吸設(shè)備 圓錐接頭 第1部分:錐頭與錐套
|
|
GB/T 1962.1-2015
|
注射器、注射針及其他醫(yī)療器械用6%(魯爾)圓錐接頭 第1部分:通用要求
|
|
ISO 18562-1:2017
|
Biocompatibility evaluation of breathing gas pathways in healthcare applications — Part 1: Evaluation and testing within a risk management process
|
|
/
|
中華人民共和國(guó)藥典(2015版)
|
注:正文中引用的上述標(biāo)準(zhǔn)以其標(biāo)準(zhǔn)號(hào)表述����。
上述標(biāo)準(zhǔn)包括了產(chǎn)品研發(fā)及注冊(cè)申報(bào)資料中經(jīng)常涉及的標(biāo)準(zhǔn)���。不包括根據(jù)產(chǎn)品的特點(diǎn)所引用的一些行業(yè)外標(biāo)準(zhǔn)或其他標(biāo)準(zhǔn)�。
產(chǎn)品適用及引用標(biāo)準(zhǔn)的審查可以分兩步來(lái)進(jìn)行���。首先對(duì)引用標(biāo)準(zhǔn)的齊全性和適宜性進(jìn)行審查��,也就是審查產(chǎn)品技術(shù)要求中與產(chǎn)品相關(guān)的[敏感詞]標(biāo)準(zhǔn)��、行業(yè)標(biāo)準(zhǔn)是否進(jìn)行了引用�,以及引用是否準(zhǔn)確。應(yīng)注意引用標(biāo)準(zhǔn)的編號(hào)���、名稱是否完整規(guī)范�����,年代號(hào)是否有效���。其次對(duì)引用標(biāo)準(zhǔn)的采納情況進(jìn)行審查。即所引用的標(biāo)準(zhǔn)中的條款要求���,是否在產(chǎn)品技術(shù)要求中進(jìn)行了實(shí)質(zhì)性的條款引用�����。這種引用通常采用兩種方式�,文字表述繁多內(nèi)容復(fù)雜的可以直接引用標(biāo)準(zhǔn)及條文號(hào)����,比較簡(jiǎn)單的也可以直接引述具體要求。
產(chǎn)品的適用范圍/預(yù)期用途
用于供電供氣不完備場(chǎng)合和緊急情況下對(duì)突發(fā)呼吸困難或呼吸衰竭的患者實(shí)施人工呼吸��、急救時(shí)提供肺通氣���。
產(chǎn)品的主要風(fēng)險(xiǎn)
1. 產(chǎn)品的風(fēng)險(xiǎn)管理報(bào)告應(yīng)符合YY/T 0316-2016《醫(yī)療器械風(fēng)險(xiǎn)管理對(duì)醫(yī)療器械的應(yīng)用》的有關(guān)要求���,判斷與產(chǎn)品有關(guān)的危險(xiǎn)�����,估計(jì)和評(píng)價(jià)相關(guān)風(fēng)險(xiǎn)�����,控制這些風(fēng)險(xiǎn)并監(jiān)視控制的有效性����。注冊(cè)申請(qǐng)人提供注冊(cè)產(chǎn)品的風(fēng)險(xiǎn)管理報(bào)告應(yīng)扼要說(shuō)明:
(1)在產(chǎn)品的研制階段���,已對(duì)其有關(guān)可能的危險(xiǎn)及產(chǎn)生的風(fēng)險(xiǎn)進(jìn)行了估計(jì)和評(píng)價(jià),并有針對(duì)性地實(shí)施了降低風(fēng)險(xiǎn)的技術(shù)和管理方面的措施�����。
(2)在產(chǎn)品性能測(cè)試部分中驗(yàn)證了這些措施的有效性�,達(dá)到了通用和相應(yīng)專用標(biāo)準(zhǔn)的要求。
(3)對(duì)所有剩余風(fēng)險(xiǎn)進(jìn)行了評(píng)價(jià)���。
(4)風(fēng)險(xiǎn)/受益分析����。
(5)對(duì)產(chǎn)品的安全性的承諾。
2. 風(fēng)險(xiǎn)管理報(bào)告的內(nèi)容至少包括:
(1)產(chǎn)品的風(fēng)險(xiǎn)管理組織�����。
(2)產(chǎn)品的組成及適用范圍��。
(3)風(fēng)險(xiǎn)報(bào)告編制的依據(jù)�����。
(4)產(chǎn)品與安全性有關(guān)的特征的判定���。
注冊(cè)申請(qǐng)人應(yīng)按照YY/T 0316-2016《醫(yī)療器械風(fēng)險(xiǎn)管理對(duì)醫(yī)療器械的應(yīng)用》附錄C的34條提示�,對(duì)照產(chǎn)品的實(shí)際情況作出針對(duì)性的簡(jiǎn)明描述�。
注意:產(chǎn)品如存在34條提示以外的可能影響安全性的特征,也應(yīng)作出說(shuō)明��。
(5)對(duì)產(chǎn)品的可能危險(xiǎn)�����、可預(yù)見(jiàn)的事件序列和危險(xiǎn)情況的判定。
注冊(cè)申請(qǐng)人應(yīng)根據(jù)自身產(chǎn)品特點(diǎn)�����,根據(jù)YY/T 0316-2016附錄E�����、I的提示���,對(duì)危險(xiǎn)�����、可預(yù)見(jiàn)的事件序列�、危險(xiǎn)情況及可發(fā)生的傷害作出判定�����。
(6)風(fēng)險(xiǎn)可接受準(zhǔn)則:降低風(fēng)險(xiǎn)的措施及采取措施后風(fēng)險(xiǎn)的可接受程度�����,是否有新的風(fēng)險(xiǎn)產(chǎn)生���。
(7)風(fēng)險(xiǎn)控制的方案與實(shí)施����、綜合剩余風(fēng)險(xiǎn)的可接受性評(píng)價(jià)及生產(chǎn)和生產(chǎn)后監(jiān)視的相關(guān)方法����,可參考YY/T 0316-2016的附錄F、G�、J。
表2 產(chǎn)品主要初始危險(xiǎn)因素
|
通用類別
|
初始事件和環(huán)境示例
|
|
不完整的要求
|
性能要求不符合���。 與人體直接接觸部件材料的生物相容性問(wèn)題�����。 說(shuō)明書(shū)未對(duì)人工復(fù)蘇器的使用操作方法進(jìn)行準(zhǔn)確的描述與說(shuō)明���。 貨架有效期不恰當(dāng)規(guī)范:在標(biāo)識(shí)的有效期前,已無(wú)法保證產(chǎn)品的性能要求����。
|
|
制造過(guò)程
|
制造過(guò)程的控制不充分:生產(chǎn)過(guò)程關(guān)鍵工序控制點(diǎn)未進(jìn)行監(jiān)測(cè)���,導(dǎo)致人工復(fù)蘇器不合格。 供方的控制不充分:外購(gòu)���、外協(xié)件供方選擇不當(dāng)�,外購(gòu)����、外協(xié)件未進(jìn)行有效進(jìn)貨檢驗(yàn),導(dǎo)致不合格外購(gòu)��、外協(xié)件投入生產(chǎn)�����。
|
|
運(yùn)輸和貯藏
|
不恰當(dāng)?shù)陌b:產(chǎn)品防護(hù)不當(dāng)導(dǎo)致產(chǎn)品運(yùn)輸過(guò)程中損壞����。 不適當(dāng)?shù)沫h(huán)境條件:產(chǎn)品存放于[敏感詞]惡劣的環(huán)境條件中,如不干凈的倉(cāng)庫(kù)���,長(zhǎng)時(shí)間高溫/低溫�����、高濕的環(huán)境�����,造成產(chǎn)品受到污染�����。
|
|
清潔��、消毒和 滅菌
|
消毒執(zhí)行不恰當(dāng):未對(duì)產(chǎn)品消毒工藝進(jìn)行確認(rèn)或未按照確認(rèn)過(guò)的參數(shù)進(jìn)行消毒�����,導(dǎo)致消毒不徹底��,產(chǎn)品有污染��。 滅菌執(zhí)行不恰當(dāng):未按要求對(duì)人工復(fù)蘇器進(jìn)行滅菌��,或未達(dá)到滅菌效果�。 重復(fù)使用次數(shù)超過(guò)經(jīng)驗(yàn)證的次數(shù)����。
|
|
處置和廢棄
|
沒(méi)提供信息或提供信息不充分:未在使用說(shuō)明書(shū)中對(duì)產(chǎn)品處置和廢棄方法進(jìn)行說(shuō)明�����,或信息不充分
|
|
材料
|
生物相容性:與人體接觸的工具部分或其他部件選擇不當(dāng)可致過(guò)敏等反應(yīng)����。 閥門(mén)老化�,密封性能問(wèn)題
|
|
人為因素
|
易混淆的或缺少使用說(shuō)明書(shū):如缺少詳細(xì)的使用方法、缺少必要的警告說(shuō)明��;使用不適當(dāng)?shù)男吞?hào)��;操作說(shuō)明過(guò)于復(fù)雜�,不易懂。 由缺乏技術(shù)的/未經(jīng)培訓(xùn)的人員使用:使用者/操作者未經(jīng)培訓(xùn)或培訓(xùn)不足���,不能正確使用人工復(fù)蘇器����。
|
表3 部分危險(xiǎn)�����、可預(yù)見(jiàn)的事件序列����、危險(xiǎn)情況和可發(fā)生的傷害之間的關(guān)系
|
危險(xiǎn)
|
可預(yù)見(jiàn)的事件序列
|
危險(xiǎn)情況
|
傷害
|
|
化學(xué)的
|
生產(chǎn)過(guò)程使用了加工助劑���,注塑過(guò)程使用了工業(yè)脫模劑等�,產(chǎn)品清潔不完全。
|
帶有化學(xué)殘留的產(chǎn)品使用于人體��。
|
刺激患者中毒���,引起炎癥��,傷害人體健康���。
|
|
生物學(xué)的 (微生物污染)
|
消毒或滅菌效果不佳;初始污染菌超標(biāo)。
|
有微生物污染的器械使用于人體
|
交叉使用�����,感染患者���,進(jìn)而感染與患者接觸的人員
|
|
生物相容性
|
產(chǎn)品無(wú)良好的生物相容性��;
|
與人體組織不相容的器械使用于人體
|
中毒�����、刺激�、過(guò)敏等癥狀,傷害患者健康�,嚴(yán)重時(shí)危及患者生命。
|
|
功能
|
進(jìn)氣閥漏氣��,無(wú)法提供足夠的輸送容量�;病人閥阻塞,氣體無(wú)法正常輸送至患者口中��;一次性使用的產(chǎn)品被重復(fù)使用��。
|
無(wú)法提供有效的肺通氣���;未進(jìn)行消毒滅菌或消毒滅菌后產(chǎn)品性能無(wú)法滿足性能要求��。
|
錯(cuò)失[敏感詞] 呼吸搶救時(shí)間�;交叉感染或無(wú)法提供有效肺通氣����。
|
表2、表3依據(jù)YY/T 0316-2016的附錄E提示性列舉了人工復(fù)蘇器可能存在危險(xiǎn)的初始事件和環(huán)境,示例性地給出了危險(xiǎn)�、可預(yù)見(jiàn)的事件序列、危險(xiǎn)情況和可發(fā)生的傷害之間的關(guān)系�����,給審查人員予以提示�、參考。
由于人工復(fù)蘇器功能和結(jié)構(gòu)的差異��,本章給出的風(fēng)險(xiǎn)要素及其示例是常見(jiàn)的而不是全部的����。上述部分只是風(fēng)險(xiǎn)管理過(guò)程的組成部分���,不是風(fēng)險(xiǎn)管理的全部��。注冊(cè)申請(qǐng)人應(yīng)按照YY/T 0316-2016中規(guī)定的過(guò)程和方法��,在產(chǎn)品整個(gè)生命周期內(nèi)建立��、形成文件和保持一個(gè)持續(xù)的過(guò)程�,用以判定與醫(yī)療器械有關(guān)的危險(xiǎn)��、估計(jì)和評(píng)價(jià)相關(guān)的風(fēng)險(xiǎn)��、控制這些風(fēng)險(xiǎn)并監(jiān)視上述控制的有效性,以充分保證產(chǎn)品的安全和有效�����。
產(chǎn)品的研究要求
1. 產(chǎn)品性能研究
應(yīng)詳述產(chǎn)品技術(shù)要求中主要性能指標(biāo)及檢驗(yàn)方法的確定依據(jù)����,提供采用的原因及理論基礎(chǔ),提供涉及的研究性資料�、文獻(xiàn)資料和標(biāo)準(zhǔn)文本。如適用的[敏感詞]標(biāo)準(zhǔn)����、行業(yè)標(biāo)準(zhǔn)中有不采納的條款,應(yīng)將不采納的條款及其理由予以闡明����。
應(yīng)研究的產(chǎn)品基本性能至少包括進(jìn)氣閥接頭、拆卸與裝配�、被嘔吐物污染的患者閥功能、機(jī)械沖擊�、增補(bǔ)氧和輸送的氧濃度、呼氣阻抗��、吸氣阻抗、死腔����、最小輸送容量、壓力限制��、微生物限度等��。
說(shuō)明書(shū)中描述的性能或產(chǎn)品宣稱的特殊性能應(yīng)進(jìn)行研究����。
若產(chǎn)品帶有配合使用的配件,應(yīng)分別列出附件的材料���、結(jié)構(gòu)、性能要求���。
應(yīng)提供產(chǎn)品的主要原材料選擇依據(jù)等信息�。
2. 生物相容性的評(píng)價(jià)研究
應(yīng)描述人工復(fù)蘇器產(chǎn)品與人體接觸部件的材料�����,以及在使用過(guò)程中與皮膚組織接觸的性質(zhì)和時(shí)間�,參照《關(guān)于印發(fā)醫(yī)療器械生物學(xué)評(píng)價(jià)和審評(píng)指南的通知》(國(guó)食藥監(jiān)械〔2007〕345號(hào))、GB/T 16886.1—2011的要求對(duì)其進(jìn)行生物相容性評(píng)價(jià)。
建議參照ISO 18562-1-2017�,對(duì)與人體間接接觸的部件進(jìn)行生物相容性評(píng)價(jià)研究。
3. 消毒或滅菌工藝研究
應(yīng)明確滅菌工藝(方法和參數(shù))和無(wú)菌保證水平(SAL)����,并提供滅菌確認(rèn)報(bào)告。若滅菌使用的方法容易出現(xiàn)殘留���,如環(huán)氧乙烷滅菌��,應(yīng)當(dāng)明確殘留物信息及采取的處理方法�����,并提供研究資料���。可根據(jù)適用情況�,按照GB 18280.1-2015、GB18280.2-2015���、 GB 18279.1-2015�、GB/T 18279.2-2015等標(biāo)準(zhǔn)的要求開(kāi)展研究�。
對(duì)于重復(fù)使用的產(chǎn)品���,應(yīng)提供終端用戶滅菌或消毒方面的研究資料,包括重復(fù)滅菌或消毒次數(shù)�����、產(chǎn)品性能的研究��。
對(duì)于使用前需要進(jìn)行清洗��、消毒或滅菌的���,應(yīng)當(dāng)明確推薦的消毒或滅菌工藝(方法和參數(shù))以及所推薦消毒/滅菌方法確定的依據(jù)�。
4. 產(chǎn)品有效期和包裝研究
(1)產(chǎn)品有效期和包裝研究情況可通過(guò)實(shí)時(shí)老化或加速老化試驗(yàn)獲得����。有效期研究項(xiàng)目包含包裝完整性和技術(shù)要求中規(guī)定的項(xiàng)目,建議選擇原材料最多�����,組件最完整����,使用性能可以覆蓋使用單元的型號(hào)進(jìn)行驗(yàn)證。加速老化試驗(yàn)可參照YY/T 0681.1—2009《無(wú)菌醫(yī)療器械包裝試驗(yàn)方法 第1部分:加速老化試驗(yàn)指南》系列標(biāo)準(zhǔn)����、GB/T 19633.1—2015《最終滅菌醫(yī)療器械包裝 第1部分:材料、無(wú)菌屏障系統(tǒng)和包裝系統(tǒng)的要求》���、GB/T 19633.2—2015《最終滅菌醫(yī)療器械包裝 第2部分:成形�����、密封和裝配過(guò)程的確認(rèn)的要求》����、YY/T 0698.1—2011《最終滅菌醫(yī)療器械包裝材料 第1部分:吸塑包裝共擠塑料膜要求和試驗(yàn)方法》系列標(biāo)準(zhǔn)等進(jìn)行���;非無(wú)菌供應(yīng)的產(chǎn)品可參考上述標(biāo)準(zhǔn)進(jìn)行有效期研究�����。
(2)申請(qǐng)人應(yīng)提交包裝研究資料�����,依據(jù)有關(guān)國(guó)內(nèi)���、國(guó)際標(biāo)準(zhǔn)(如GB/T 19633.1-2015���、GB/T 19633.2-2015、ISO 11607-1等)對(duì)包裝進(jìn)行分析研究和評(píng)價(jià)�。直接接觸產(chǎn)品的包裝材料的選擇應(yīng)至少考慮以下因素:包裝材料的物理化學(xué)性能;包裝材料的毒理學(xué)特性�;包裝材料與產(chǎn)品的適應(yīng)性;包裝材料與成型和密封過(guò)程的適應(yīng)性��;包裝材料與滅菌過(guò)程的適應(yīng)性���;包裝材料所能提供的物理����、化學(xué)和微生物屏障保護(hù)�;包裝材料與使用者使用時(shí)的要求(如無(wú)菌開(kāi)啟)的適應(yīng)性;包裝材料與標(biāo)簽系統(tǒng)的適應(yīng)性��;包裝材料與貯存運(yùn)輸過(guò)程的適應(yīng)性�;非無(wú)菌供應(yīng)的產(chǎn)品,可參考上述適用的項(xiàng)目進(jìn)行包裝研究��。
產(chǎn)品技術(shù)要求應(yīng)包括的主要性能指標(biāo)
人工復(fù)蘇器產(chǎn)品有直接對(duì)應(yīng)的行業(yè)標(biāo)準(zhǔn)YY 0600.4-2013《醫(yī)用呼吸機(jī) 基本安全和主要性能專用要求 第4部分:人工復(fù)蘇器》�,對(duì)產(chǎn)品本身明確了要求。不同企業(yè)可根據(jù)自身產(chǎn)品的技術(shù)特點(diǎn)制定性能指標(biāo)要求��,但不得低于相關(guān)強(qiáng)制性標(biāo)準(zhǔn)的強(qiáng)制性要求����、說(shuō)明書(shū)中描述的性能或產(chǎn)品宣稱的特殊性能應(yīng)進(jìn)行研究。
物理性能:
1. 患者連接口接頭
2. 呼吸氣體的呼氣口接頭
3. 面罩接頭
4. 氣囊充氣閥接頭
5. 氣囊進(jìn)氣閥接頭
6. 螺紋氣體過(guò)濾器接頭
7. 氧氣管接頭和壓力計(jì)接頭
8. 操作要求
8.1 拆卸和裝配
8.2 被嘔吐物污染后的患者閥功能
9. 機(jī)械沖擊
9.1 墜落試驗(yàn)
9.2 浸水
9.3 氣囊充氣閥
10. 增補(bǔ)氧和輸送的氧濃度
11. 呼氣阻抗
12. 吸氣阻抗
13. 患者閥故障
14. 患者閥泄漏—前向泄漏
15. 人工復(fù)蘇器死腔和重復(fù)呼吸
16. 通氣性能
16.1最小輸送容量
16.2 壓力限制
17. 儲(chǔ)存和操作條件
18. 壓力限制系統(tǒng)設(shè)置的指示��。
19. 外觀要求�����。
20. 若產(chǎn)品包含其他配合使用的附件�����,應(yīng)結(jié)合產(chǎn)品功能�、結(jié)構(gòu)制定相關(guān)性能要求。例如��,儲(chǔ)氣袋性能要求(接頭�、容量、外觀�����、氣密性)。
21. 化學(xué)性能
根據(jù)不同材料特性�����,由申請(qǐng)人決定是否對(duì)化學(xué)性能提出要求����。跟人體直接接觸的部件,應(yīng)補(bǔ)充化學(xué)性能的要求(至少pH值����、重金屬)。
22. 生物性能
22.1 非無(wú)菌供應(yīng)的產(chǎn)品���,若產(chǎn)品首次使用前不需要進(jìn)行清洗�、消毒�����、滅菌處理��,鼓勵(lì)申請(qǐng)人對(duì)微生物限度進(jìn)行規(guī)定��。
22.2 以滅菌包裝提供的產(chǎn)品應(yīng)無(wú)菌。
22.3 采用環(huán)氧乙烷滅菌的產(chǎn)品�����,環(huán)氧乙烷殘留量不得大于10μg/g�����。
檢測(cè)單元中典型產(chǎn)品的確定原則和實(shí)例
同一注冊(cè)單元應(yīng)按產(chǎn)品風(fēng)險(xiǎn)與技術(shù)指標(biāo)的覆蓋性來(lái)選擇典型產(chǎn)品�����。典型產(chǎn)品應(yīng)是同一注冊(cè)單元內(nèi)能夠代表本單元內(nèi)其他產(chǎn)品安全性和有效性的產(chǎn)品�,應(yīng)考慮功能最齊全��、結(jié)構(gòu)最復(fù)雜�、原材料最多的產(chǎn)品,若不能完全覆蓋���,還應(yīng)選擇其他型號(hào)進(jìn)行差異性檢驗(yàn)���。例如:病人閥、進(jìn)氣閥結(jié)構(gòu)不同的��,應(yīng)分別進(jìn)行檢驗(yàn)。
產(chǎn)品生產(chǎn)制造相關(guān)要求
1. 應(yīng)當(dāng)明確人工復(fù)蘇器生產(chǎn)工藝流程����,注明關(guān)鍵工序和特殊過(guò)程,并說(shuō)明其過(guò)程控制點(diǎn)�����。
2. 有多個(gè)研制���、生產(chǎn)場(chǎng)地����,應(yīng)當(dāng)概述每個(gè)研制�����、生產(chǎn)場(chǎng)地的實(shí)際情況��,相關(guān)的生產(chǎn)環(huán)境應(yīng)符合《醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范》([敏感詞]食品藥品監(jiān)督管理總局公告2014年第64號(hào))的相關(guān)要求和YY/T 0287—2017的相關(guān)要求����。
產(chǎn)品的臨床評(píng)價(jià)要求
按照《醫(yī)療器械臨床評(píng)價(jià)技術(shù)指導(dǎo)原則》([敏感詞]食品藥品監(jiān)督管理總局通告2015年第14號(hào))提交臨床評(píng)價(jià)資料。
與《免于進(jìn)行臨床試驗(yàn)的醫(yī)療器械目錄(修訂)》([敏感詞]藥品監(jiān)督管理局通告2018年第94號(hào)���,以下簡(jiǎn)稱《目錄》)中���,序號(hào)為340“人工復(fù)蘇器(人工復(fù)蘇器)”相同的產(chǎn)品可免于進(jìn)行臨床試驗(yàn)�����。申請(qǐng)人需提交申報(bào)產(chǎn)品相關(guān)信息與《目錄》所述內(nèi)容的對(duì)比資料和申報(bào)產(chǎn)品與已獲準(zhǔn)境內(nèi)注冊(cè)的《目錄》中醫(yī)療器械的對(duì)比說(shuō)明。
若無(wú)法證明申報(bào)產(chǎn)品與《目錄》產(chǎn)品具有等同性���,則應(yīng)按照《醫(yī)療器械臨床評(píng)價(jià)技術(shù)審查指導(dǎo)原則》及其他臨床評(píng)價(jià)法規(guī)文件的要求開(kāi)展相應(yīng)工作�����,提供符合要求的臨床評(píng)價(jià)資料�����。
產(chǎn)品的不良事件歷史記錄
暫未查詢到人工復(fù)蘇器臨床使用出現(xiàn)不良事件的信息���。
產(chǎn)品說(shuō)明書(shū)和標(biāo)簽要求
產(chǎn)品說(shuō)明書(shū)、標(biāo)簽的編寫(xiě)要求應(yīng)符合《醫(yī)療器械說(shuō)明書(shū)和標(biāo)簽管理規(guī)定》([敏感詞]食品藥品監(jiān)督管理總局令第6號(hào))�、YY/T 0466.1—2016、YY/T 0313—2014��、YY 0600.4-2013等相關(guān)標(biāo)準(zhǔn)的要求。同時(shí)應(yīng)注意以下要求�����。
1. 在所有預(yù)期操作模式下�����,如何操作人工復(fù)蘇器的說(shuō)明�����。
2. 每個(gè)型號(hào)適合使用的體重范圍����。
3. 操作環(huán)境、儲(chǔ)存環(huán)境限制�。
4. 除空氣外,人工復(fù)蘇器能輸送的所有內(nèi)容物��。
5. 能輸送的氧濃度����。
6. 輸送氣體容量范圍。
7. 人工復(fù)蘇器死腔�����、前向泄漏和反向泄漏。
8. 呼氣阻抗�、吸氣阻抗和使用推薦附件所加的阻抗。
9. 人工復(fù)蘇器正常使用時(shí)產(chǎn)生的呼末壓�,如果大于0.2kPa,應(yīng)說(shuō)明�。
10. 如果有壓力限制系統(tǒng)和超控裝置,應(yīng)說(shuō)明其詳細(xì)信息�����。
11. 如果人工復(fù)蘇器配有控制裝置或指示裝置�,應(yīng)說(shuō)明其準(zhǔn)確性��。
12. 為了清潔而需拆卸和裝配的說(shuō)明��,以及裝配后進(jìn)行操作的性能測(cè)試的詳細(xì)說(shuō)明���。
13. 對(duì)人工復(fù)蘇器���、部件、配件進(jìn)行清潔�、消毒或滅菌的推薦方法��。
14. 使用前需進(jìn)行的功能測(cè)試�。
15. 維護(hù)要求���。
16. 在有害或有毒環(huán)境中使用的建議(如適用)�。
17. 操作者可更換的部件清單�����。
18. 在高氧濃度條件下��,煙和火會(huì)引起危險(xiǎn)的警告���,以及人工復(fù)蘇器禁止使用油脂的警告�����。
19. 警告不正確的使用人工復(fù)蘇器會(huì)造成危險(xiǎn)�����。
20. 一次性使用產(chǎn)品應(yīng)當(dāng)注明是“一次性使用”或“禁止重復(fù)使用”字樣或符號(hào)�����。
21. 產(chǎn)品使用后需要處理的����,應(yīng)當(dāng)標(biāo)明相應(yīng)的處理辦法。
22. 有限次重復(fù)使用的產(chǎn)品應(yīng)注明可供使用的次數(shù)和建議的消毒或滅菌方式����。
23. 明確本產(chǎn)品為一次性使用或僅限同一個(gè)人使用,若僅限同一個(gè)人使用應(yīng)描述其風(fēng)險(xiǎn)及處理方法�。
審查關(guān)注點(diǎn)
(一)重點(diǎn)關(guān)注產(chǎn)品技術(shù)要求編寫(xiě)的規(guī)范性,引用標(biāo)準(zhǔn)的適用性�����、準(zhǔn)確性����、有效性�,是否結(jié)合產(chǎn)品所含的選配件制定相應(yīng)的性能指標(biāo)。
(二)重點(diǎn)關(guān)注注冊(cè)申請(qǐng)人的產(chǎn)品研究資料是否全面����、準(zhǔn)確,是否體現(xiàn)其安全性����、有效性���。
(三)重復(fù)使用器械:技術(shù)審評(píng)時(shí)需特別關(guān)注重復(fù)使用次數(shù)的驗(yàn)證,清洗和消毒方法的確認(rèn)�����。
(四)產(chǎn)品檢驗(yàn)報(bào)告:應(yīng)關(guān)注檢測(cè)的典型型號(hào)是否覆蓋所有性能要求���,檢驗(yàn)報(bào)告所附照片中的產(chǎn)品結(jié)構(gòu)組成���、標(biāo)識(shí)標(biāo)簽等信息,是否與其他申報(bào)資料描述相同�。
(五)對(duì)說(shuō)明書(shū)的審查應(yīng)注意明確產(chǎn)品的信息,選配件應(yīng)列明并表述正確��。